Valvulopatía
| Valvulopatía | ||
|---|---|---|
 | ||
| Especialidad | genética médica | |
Las valvulopatías son todas aquellas enfermedades que afectan a las válvulas cardíacas, independientemente de su etiología o la gravedad del cuadro clínico que produzcan. Cualquiera de las válvulas del corazón: aórtica o mitral en el lado izquierdo y válvula pulmonar o válvula tricúspide en el lado derecho, pueden obstruirse o presentar regurgitación de sangre a la cámara de procedencia bien de la aurícula o del ventrículo.
Las valvulopatías pueden ser congénitas, presentes en el momento del nacimiento,[1] en cuyo caso se suelen denominar displasia valvular, o adquiridas a lo largo de la vida.[2] La valvulopatía más frecuente es la estenosis aórtica. El tratamiento depende de la severidad del trastorno e incluye la utilización de determinados medicamentos o bien el reemplazo de la válvula afectada por una artificial.[3][4]
Anatómicamente, las válvulas forman parte del denso tejido conectivo del corazón conocido como esqueleto cardíaco y son responsables de la regulación del flujo sanguíneo a través del corazón y los grandes vasos. La insuficiencia o disfunción de las válvulas puede dar lugar a una disminución de la funcionalidad del corazón, aunque las consecuencias particulares dependen del tipo y la gravedad de la enfermedad valvular. El tratamiento de las válvulas dañadas puede implicar la medicación sola, pero a menudo implica la reparación quirúrgica de la válvula (valvuloplastia) o su sustitución (inserción de una válvula cardíaca artificial).
Causas
[editar]Las causas más frecuentes de valvulopatía son la fiebre reumática, los procesos degenerativos debidos a la edad y las anomalías congénitas del corazón que provocan alteraciones en la formación de las válvulas en el periodo embrionario, en este caso la afección recibe generalmente el nombre de displasia valvular.[4]
Clasificación
[editar]
Si el problema radica en una disminución permanente del diámetro del orificio valvular, se denomina (estenosis) valvular, cuando existe disminución de la capacidad de la válvula para cerrarse se llama insuficiencia valvular, si existe un movimiento de las válvulas en sentido anómalo se designa como prolapso valvular.
La estenosis y la insuficiencia/regurgitación representan las consecuencias funcionales y anatómicas dominantes asociadas a la enfermedad valvular cardíaca. Independientemente del proceso de la enfermedad, se producen alteraciones en la válvula que producen una o una combinación de estas condiciones. Insuficiencia y regurgitación son términos sinónimos que describen la incapacidad de la válvula para evitar el reflujo de sangre cuando las valvas de la válvula no se unen (coaptan) correctamente. La estenosis se caracteriza por un estrechamiento del orificio valvular que impide la salida adecuada de la sangre. La estenosis también puede dar lugar a una insuficiencia si el engrosamiento del anillo o de las valvas da lugar a un cierre inadecuado de las hojas.
| Válvula afectada | Trastorno obstructivo | Insuficiencia valvular |
| Válvula aórtica | Estenosis aórtica | Insuficiencia aórtica o regurgitación |
| Válvula mitral | Estenosis mitral y prolapso mitral | Insuficiencia mitral o regurgitación |
| Válvula tricuspídea | Estenosis tricuspídea | Insuficiencia tricuspídea o regurgitación |
| Válvula pulmonar | Estenosis pulmonar | Insuficiencia pulmonar o regurgitación |
Cuadro clínico
[editar]La clínica y la evolución de cada cuadro es muy variable, atendiendo a la válvula afectada y la causa subyacente. Muchas veces el tratamiento sintomático es suficiente, mientras que en otros casos se hace necesario el recambio valvular mediante cirugía.
Trastornos de la válvula aórtica y mitral
[editar]La enfermedad de la válvula aórtica y mitral se denominan enfermedades del corazón izquierdo. Las enfermedades de estas válvulas son más frecuentes que las de la válvula pulmonar o tricúspide debido a las mayores presiones que experimenta el corazón izquierdo.[5]
La estenosis de la válvula aórtica se caracteriza por un engrosamiento del anillo o las valvas valvulares que limita la capacidad de la sangre para ser expulsada del ventrículo izquierdo hacia la aorta. La estenosis es típicamente el resultado de la calcificación valvular, pero puede ser el resultado de una malformación congénita de la válvula aórtica bicúspide. Este defecto se caracteriza por la presencia de sólo dos valvas. Puede ocurrir de forma aislada o en conjunto con otras anomalías cardíacas.
La insuficiencia aórtica, o regurgitación, se caracteriza por la incapacidad de las valvas para cerrar adecuadamente al final de la sístole, permitiendo así que la sangre fluya inadecuadamente hacia atrás en el ventrículo izquierdo. Las causas de la insuficiencia aórtica en la mayoría de los casos son desconocidas o idiopáticas.[6] Puede ser el resultado de trastornos del tejido conectivo o inmunológicos, como el síndrome de Marfan o el lupus eritematoso sistémico, respectivamente. Los procesos que conducen a la insuficiencia aórtica suelen implicar la dilatación del anillo de la válvula, desplazando así las valvas, que están ancladas en el anillo.
La estenosis mitral es causada en gran parte por la enfermedad cardiaca reumática, aunque rara vez es el resultado de la calcificación. En algunos casos se forman vegetaciones en las valvas mitrales como resultado de la endocarditis, una inflamación del tejido del corazón. La estenosis mitral es poco común y no depende tanto de la edad como otros tipos de enfermedades valvulares.[5]
La insuficiencia mitral puede ser causada por la dilatación del corazón izquierdo, a menudo una consecuencia de la insuficiencia cardíaca. En estos casos el ventrículo izquierdo del corazón se agranda y causa el desplazamiento de los músculos papilares adjuntos, que controlan la válvula mitral.
Trastornos pulmonares y de la válvula tricúspide
[editar]Las enfermedades pulmonares y de la válvula tricúspide son enfermedades del corazón derecho. Las enfermedades de la válvula pulmonar son las menos comunes en los adultos.[1][5] La estenosis de la válvula pulmonar suele ser el resultado de malformaciones congénitas y se observa de forma aislada o como parte de un proceso patológico más amplio, como en la tetralogía de Fallot, el síndrome de Noonan y el síndrome de rubéola congénita. A menos que el grado de estenosis sea grave, los individuos con estenosis pulmonar suelen tener excelentes resultados y opciones de tratamiento. A menudo los pacientes no requieren intervención hasta más tarde en la edad adulta como consecuencia de la calcificación que ocurre con el envejecimiento.
La insuficiencia de la válvula pulmonar se produce comúnmente en individuos sanos en una medida muy leve y no requiere intervención.[7] Una insuficiencia más apreciable es típicamente el resultado de un daño en la válvula debido a un cateterismo cardíaco, la inserción de una bomba de balón intraaórtica u otras manipulaciones quirúrgicas. Además, la insuficiencia puede ser el resultado del síndrome carcinoide, procesos inflamatorios como la enfermedad reumatoide o la endocarditis, o malformaciones congénitas.[8][9] También puede ser secundaria a la hipertensión pulmonar grave.
La estenosis de la válvula tricúspide sin regurgitación co-ocurrente es muy poco común y normalmente es el resultado de una enfermedad reumática. También puede ser el resultado de anormalidades congénitas, síndrome carcinoide, tumores obstructivos de la aurícula derecha (típicamente lipomas o mixomas) o síndromes hipereosinofílicos.
La insuficiencia tricúspide menor es común en individuos sanos.[10] En casos más graves es una consecuencia de la dilatación del ventrículo derecho, que lleva al desplazamiento de los músculos papilares que controlan la capacidad de la válvula para cerrarse.[11] La dilatación del ventrículo derecho se produce como consecuencia de defectos septales ventriculares, derivación de sangre de derecha a izquierda, síndrome de Eisenmenger, hipertiroidismo y estenosis pulmonar. La insuficiencia tricúspide también puede ser el resultado de defectos congénitos de la válvula tricúspide, como la anomalía de Ebstein.
Signos y síntomas
[editar]Estenosis aórtica
[editar]Los síntomas de la estenosis aórtica pueden incluir síntomas de insuficiencia cardíaca, como la disnea por esfuerzo (el síntoma más frecuente),[12] la ortopnea y la disnea paroxística nocturna,[13] la angina de pecho[13] y el síncope, generalmente por esfuerzo.[13]
Los signos médicos de la estenosis aórtica incluyen pulsus parvus et tardus, es decir, disminución y retraso del pulso carotídeo,[13][12] cuarto sonido cardíaco,[13] disminución del sonido A2,[12] latido ápice sostenido[13] y emoción precordial.[12] La auscultación puede revelar un soplo sistólico de tipo duro crescendo-decrescendo, que se oye en el segundo espacio intercostal derecho[12] e irradia a las arterias carótidas.[13]
Regurgitación aórtica
[editar]Los pacientes con regurgitación aórtica pueden experimentar síntomas de insuficiencia cardíaca, como disnea por esfuerzo, ortopnea y disnea paroxística nocturna, palpitaciones y angina de pecho.[13] En los casos agudos los pacientes pueden experimentar cianosis y shock circulatorio.[13]
Los signos médicos de la regurgitación aórtica incluyen el aumento de la presión del pulso por el aumento de la presión sanguínea sistólica y la disminución de la presión sanguínea diastólica.[13] El paciente puede tener un soplo diastólico en decrescendo que se escucha mejor en el borde esternal izquierdo, pulso de martillo de agua, soplo de Austin Flint y un latido de ápice desplazado hacia abajo y a la izquierda.[13] Puede estar presente un tercer sonido cardíaco.[13]
Estenosis mitral
[editar]Los pacientes con estenosis mitral pueden presentar síntomas de insuficiencia cardíaca, como disnea por esfuerzo, ortopnea y disnea paroxística nocturna, palpitaciones, dolor en el pecho, hemoptisis, tromboembolia o ascitis y edema (si se desarrolla una insuficiencia cardíaca del lado derecho).[13] Los síntomas de la estenosis mitral aumentan con el ejercicio y el embarazo.[13]
En la auscultación de un paciente con estenosis mitral, típicamente el signo más prominente es un fuerte S1.[13] Otro hallazgo es un chasquido de apertura seguido de un estruendo diastólico de tono bajo con acentuación presistólica.[13][12] El chasquido de apertura sigue más cerca del tono cardíaco S2 con empeoramiento de la estenosis.[13] El soplo se escucha mejor con la campana del estetoscopio[13] situada en el lado izquierdo[12] y su duración aumenta con el empeoramiento de la enfermedad.[13] La enfermedad avanzada puede presentar signos de insuficiencia cardíaca del lado derecho, como el derrame parasternal, la distensión venosa yugular, la hepatomegalia, la ascitis y/o la hipertensión pulmonar (que se presenta con un fuerte P2).[13] Los signos aumentan con el ejercicio y el embarazo.[13]
Regurgitación mitral
[editar]Los pacientes con regurgitación mitral pueden presentar síntomas de insuficiencia cardíaca, como disnea por esfuerzo, ortopnea y disnea paroxística nocturna,[13] palpitaciones[13] o edema pulmonar.[13]
En la auscultación de un paciente con estenosis mitral, puede haber un soplo holosistólico en el ápice, que se irradia a la espalda o a la zona clavicular,[13] un tercer sonido cardíaco,[13] y un fuerte y palpable P2,[13] que se escucha mejor cuando se está tumbado sobre el lado izquierdo.[12] Los pacientes también suelen tener fibrilación auricular.[13] Los pacientes pueden tener un latido del ápice desplazado lateralmente,[13] a menudo con un tirón.[12] En los casos agudos, el soplo y la taquicardia pueden ser sólo signos distintivos.[12]
Regurgitación tricuspídea
[editar]Los pacientes con regurgitación tricuspídea pueden experimentar síntomas de insuficiencia cardíaca derecha, como ascitis, hepatomegalia, edema y distensión venosa yugular.[13]
Entre los signos de regurgitación tricuspídea se incluyen el hígado pulsátil, las ondas V prominentes y los rápidos descensos y en la presión venosa yugular.[13] Los hallazgos auscultatorios incluyen un tercer sonido cardíaco inspiratorio en el borde inferior izquierdo del esternón (LLSB)[13] y un soplo holosistólico en el LLSB, que se intensifica con la inspiración y disminuye con la expiración y la maniobra de Valsalva.[13] Los pacientes pueden tener un soplo parasternal a lo largo del LLSB.[13] La fibrilación auricular se presenta generalmente en pacientes con regurgitación tricuspídea.[13]
Diagnóstico
[editar]Estenosis aórtica
[editar]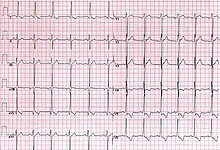
Los pacientes con estenosis aórtica pueden tener hallazgos en la radiografía de tórax que muestren la dilatación de la aorta ascendente, pero también pueden tener una radiografía de tórax completamente normal.[14] La visualización directa de las calcificaciones en la radiografía de tórax es poco común.[14] Otros hallazgos incluyen la dilatación del ventrículo izquierdo.[14] El ECG típicamente muestra la hipertrofia del ventrículo izquierdo en pacientes con estenosis severa, pero también puede mostrar signos de esfuerzo del corazón izquierdo.[15] La ecocardiografía es el estándar de oro del diagnóstico, que muestra la hipertrofia del ventrículo izquierdo, la calcificación de los folículos y el cierre anormal de los mismos.[15]
| Clasificación | Área de la válvula |
|---|---|
| Estenosis aórtica leve | 1,5-2,0 cm² |
| Estenosis aórtica moderada | 1,0-1,5 cm² |
| Estenosis aórtica severa | <1 cm² |
Regurgitación aórtica
[editar]La radiografía de tórax no es tan sensible como otras pruebas, pero puede mostrar la dilatación de la raíz aórtica (especialmente en las causas que involucran a la raíz aórtica) y el desplazamiento del ápice.[17] El ECG puede mostrar la hipertrofia del ventrículo izquierdo y signos de esfuerzo del corazón izquierdo.[17] La desviación del eje izquierdo puede ser un signo de enfermedad avanzada.[17] El ecocardiograma puede ser útil para determinar la causa de la enfermedad, ya que mostrará claramente la dilatación o disección de la raíz aórtica si existe.[17] Típicamente la función de bombeo del corazón durante la sístole es normal, pero el ecocardiograma mostrará la inversión del flujo durante la diástole.[17] Esta enfermedad se clasifica utilizando la fracción regurgitante (RF por sus siglas en inglés: Regurgitant Fraction), o el volumen que fluye de regreso a través de la válvula dividido por el flujo total hacia adelante a través de la válvula durante la sístole. La enfermedad grave tiene un RF de >50 %, mientras que la regurgitación aórtica progresiva tiene un RF de 30-49 %.[7]
Estenosis mitral
[editar]La radiografía de tórax en la estenosis mitral mostrará típicamente un agrandamiento de la aurícula izquierda, y puede mostrar la dilatación de las venas pulmonares.[18] El ECG puede mostrar el agrandamiento de la aurícula izquierda, debido al aumento de las presiones en la misma.[18] La ecocardiografía es útil para determinar la gravedad de la enfermedad al estimar la presión sistólica de la arteria pulmonar.[18] Esta prueba también puede mostrar la calcificación de la valva y el gradiente de presión sobre la válvula mitral.[18] La estenosis mitral severa se define como un área de la válvula mitral <1,5 cm².[7] La estenosis mitral progresiva tiene un área valvular normal, pero tendrá un aumento de la velocidad del flujo a través de la válvula mitral.[7]
Regurgitación mitral
[editar]La radiografía de tórax en la regurgitación mitral puede mostrar un agrandamiento de la aurícula izquierda, así como congestión venosa pulmonar.[19] También puede mostrar calcificaciones valvulares específicamente en la combinación de regurgitación mitral y estenosis debido a enfermedad cardiaca reumática.[19] El ECG típicamente muestra el agrandamiento de la aurícula izquierda, pero también puede mostrar el agrandamiento de la aurícula derecha si la enfermedad es lo suficientemente severa como para causar hipertensión pulmonar. La ecocardiografía es útil para visualizar el flujo regurgitante y calcular el RF.[19] También se puede utilizar para determinar el grado de calcificación, y la función y cierre de las valvas.[19] La enfermedad grave tiene un RF de >50 %, mientras que la regurgitación mitral progresiva tiene un RF de <50 %.
Causas y factores de riesgo
[editar]Calcificación
[editar]La calcificación de las valvas de la válvula aórtica es común con el aumento de la edad, pero es probable que el mecanismo esté más relacionado con el aumento de los depósitos de lipoproteínas y la inflamación que con el "desgaste" de la edad avanzada.[20] La estenosis aórtica debida a la calcificación de la válvula aórtica tricúspide con la edad[13] comprende >50 % de los afectados por la enfermedad. La estenosis aórtica debida a la calcificación de la válvula aórtica bicúspide[13] comprende alrededor del 30-40 %[12] de los afectados por la enfermedad. La hipertensión, la diabetes mellitus, la hiperlipoproteinemia y la uremia pueden acelerar el proceso de calcificación valvular.[12]
Displasia
[editar]La displasia de la válvula cardíaca es un error en el desarrollo de cualquiera de las válvulas cardíacas, y una causa común de defectos cardíacos congénitos tanto en humanos como en animales; la tetralogía de Fallot es un defecto cardíaco congénito con cuatro anomalías, una de las cuales es la estenosis de la válvula pulmonar. La anomalía de Ebstein es una anormalidad de la válvula tricúspide, y su presencia puede conducir a la regurgitación de la válvula tricúspide.[13][3]
Una válvula aórtica bicúspide[13] es una válvula aórtica con sólo 2 cúspides en lugar de las 3 normales. Está presente en alrededor del 0,5 % al 2 % de la población general, y causa un aumento de la calcificación debido a un mayor flujo turbulento a través de la válvula.[20]
Trastornos del tejido conectivo
[editar]El síndrome de Marfan es un trastorno del tejido conectivo que puede conducir a una regurgitación aórtica o mitral crónica.[13] La osteogénesis imperfecta es un trastorno en la formación de colágeno de tipo I y también puede conducir a una regurgitación aórtica crónica.[13]
Trastornos inflamatorios
[editar]La inflamación de las válvulas cardíacas por cualquier causa se llama endocarditis valvular; esto se debe generalmente a una infección bacteriana, pero también puede deberse al cáncer (endocarditis marántica), a ciertas condiciones autoinmunes (endocarditis de Libman-Sacks, vista en lupus eritematoso sistémico) y en el síndrome hipereosinofílico (endocarditis de Loeffler). La endocarditis de las válvulas puede conducir a la regurgitación a través de esa válvula, que se observa en las válvulas tricúspide, mitral y aórtica.[13] Ciertos medicamentos se han asociado con la enfermedad valvular cardíaca, sobre todo los derivados de la ergotamina pergolida y cabergolina.[21]
La enfermedad valvular cardíaca resultante de la fiebre reumática se conoce como enfermedad cardíaca reumática. El daño a las válvulas cardíacas se produce después de una infección con bacterias beta-hemolíticas, como las típicas del tracto respiratorio. La patogénesis depende de la reacción cruzada de las proteínas M producidas por las bacterias con el miocardio.[22] Esto da lugar a una inflamación generalizada en el corazón, que se manifiesta en la válvula mitral como vegetaciones, y el engrosamiento o fusión de las valvas, lo que lleva a una válvula de ojal gravemente comprometida.
La enfermedad cardiaca reumática típicamente sólo involucra la válvula mitral (70 % de los casos), aunque en algunos casos las válvulas aórtica y mitral están ambas involucradas (25 %). La implicación de otras válvulas cardíacas sin dañar la mitral es extremadamente rara.[22] La estenosis mitral casi siempre es causada por una enfermedad cardíaca reumática.[13] Menos del 10 % de la estenosis aórtica es causada por una enfermedad cardíaca reumática.[13][12] La fiebre reumática también puede causar una regurgitación mitral y aórtica crónica.[13]
Si bien los países desarrollados tuvieron en su día una importante carga de fiebre reumática y enfermedades cardíacas reumáticas, los avances médicos y la mejora de las condiciones sociales han reducido drásticamente su incidencia. Muchos países en desarrollo, así como las poblaciones indígenas de los países desarrollados, siguen soportando una carga importante de fiebre reumática y enfermedades cardíacas reumáticas, y se ha producido un resurgimiento de los esfuerzos por erradicar las enfermedades en esas poblaciones.
Las enfermedades de la raíz aórtica pueden causar una regurgitación aórtica crónica. Estas enfermedades incluyen aortitis sifilítica, enfermedad de Behçet, y artritis reactiva.[13]
Enfermedad cardíaca
[editar]La regurgitación tricuspídea suele ser secundaria a la dilatación del ventrículo derecho[13] que puede deberse a una insuficiencia del ventrículo izquierdo (la causa más común), un infarto del ventrículo derecho, infarto de miocardio inferior[13] o cor pulmonale.[13] Otras causas de regurgitación tricuspídea son el síndrome carcinoide y degeneración mixomatosa.[13]
Poblaciones especiales
[editar]Embarazo
[editar]La evaluación de las personas con valvulopatía cardíaca que están o desean quedar embarazadas es una cuestión difícil. Entre los temas que deben abordarse se encuentran los riesgos durante el embarazo para la madre y el feto en desarrollo por la presencia de la valvulopatía cardíaca materna como enfermedad intercurrente en el embarazo. Los cambios fisiológicos normales durante el embarazo requieren, en promedio, un aumento del 50 % del volumen sanguíneo circulante que va acompañado de un aumento del gasto cardíaco que suele alcanzar su punto máximo entre la porción media del segundo y tercer trimestre.[23] El aumento del gasto cardíaco se debe a un aumento en el volumen sistólico y un pequeño aumento en la frecuencia cardíaca, con un promedio de 10 a 20 latidos por minuto.[23] Además, la circulación uterina y las hormonas endógenas hacen que disminuya la resistencia vascular sistémica y una disminución desproporcionada de la presión arterial diastólica provoca una presión de pulso amplia.[23] La obstrucción de la vena cava inferior por un útero grávido en posición supina puede provocar una disminución brusca de la precarga cardíaca, lo que conduce a hipotensión con debilidad y aturdimiento.[23] Durante el preparto y el parto el gasto cardíaco aumenta más en parte debido a la ansiedad y el dolor asociados, así como debido a las contracciones uterinas que causarán un aumento de la presión sanguínea sistólica y diastólica.[23]
Las lesiones valvulares cardíacas asociadas con un alto riesgo materno y fetal durante el embarazo incluyen:[23]
- Estenosis aórtica grave con o sin síntomas
- Regurgitación aórtica con síntomas de clase funcional III-IV de la NYHA
- Estenosis mitral con síntomas de clase funcional II-IV de la NYHA
- Regurgitación mitral con síntomas de clase funcional III-IV de la NYHA
- Enfermedad de la válvula aórtica y/o mitral que resulta en una severa hipertensión pulmonar (presión pulmonar mayor al 75 % de las presiones sistémicas)
- Enfermedad de la válvula aórtica y/o mitral con disfunción grave del VI (EF menos de 0,40)
- Válvula protésica mecánica que requiere anticoagulación
- Síndrome de Marfan con o sin regurgitación aórtica[23]
En los individuos que requieren una válvula cardíaca artificial, se debe considerar el deterioro de la válvula con el tiempo (en el caso de las válvulas bioprotésicas) frente a los riesgos de coagulación de la sangre en el embarazo con válvulas mecánicas con la consiguiente necesidad de medicamentos en el embarazo en forma de anticoagulación.
Tratamiento
[editar]Algunos de los tratamientos más comunes de la valvulopatía cardíaca son evitar el tabaco y el consumo excesivo de alcohol, antibióticos, medicamentos antitrombóticos como la aspirina, anticoagulantes, dilatación con balón y diuréticos.
En algunos casos, puede ser necesaria la cirugía.
Estenosis aórtica
[editar]El tratamiento de la estenosis aórtica no es necesario en pacientes asintomáticos, a menos que la estenosis se clasifique como grave basándose en la hemodinámica de la válvula.[7] Tanto la estenosis aórtica asintomática grave como la sintomática se tratan con una cirugía de reemplazo de la válvula aórtica (AVR por sus siglas en inglés Aortic Valve Replacement).[7] El reemplazo de la válvula aórtica trans-catéter (TAVR) es una alternativa a la AVR y se recomienda en pacientes de alto riesgo que pueden no ser aptos para la AVR quirúrgica.[24] Cualquier angina se trata con nitrovasodilatadores de corta acción, beta-bloqueadores y/o bloqueadores de calcio. Cualquier hipertensión es tratada agresivamente, pero se debe tener precaución en la administración de beta-bloqueadores.[12] Cualquier insuficiencia cardíaca es tratada con digoxina, diuréticos, nitrovasodilatadores y, si no está contraindicada, se debe tener precaución en la administración hospitalaria de inhibidores de la ECA.[12] Las estenosis moderadas son monitoreadas con ecocardiografía cada 1-2 años, posiblemente con una prueba de esfuerzo cardíaco suplementaria.[12] Las estenosis severas deben ser monitoreadas con ecocardiografía cada 3-6 meses.[12]
Regurgitación aórtica
[editar]La regurgitación aórtica se trata con el reemplazo de la válvula aórtica, que se recomienda en pacientes con regurgitación aórtica grave sintomática.[7] El reemplazo de la válvula aórtica también se recomienda en pacientes asintomáticos pero con regurgitación aórtica grave crónica y una fracción de eyección del ventrículo izquierdo inferior al 50 %.[7] La hipertensión se trata en pacientes con regurgitación aórtica crónica, siendo los antihipertensivos de elección los bloqueadores de los canales de calcio, los inhibidores de la ECA o los BRA.[7] Además, la profilaxis de la endocarditis está indicada antes de procedimientos dentales, gastrointestinales o genitourinarios.[13]
La regurgitación aórtica de leve a moderada debe ser seguida de una ecocardiografía y una prueba de esfuerzo cardíaco una vez cada 1-2 años.[12] En casos severos moderados/graves, los pacientes deben ser seguidos con ecocardiografía y prueba de esfuerzo cardíaco y/o imagen de perfusión isotópica cada 3-6 meses.[12]
Estenosis mitral
[editar]Para los pacientes con estenosis mitral sintomática grave, se recomienda la valvuloplastia mitral con balón percutáneo (PBMV por sus siglas en inglés Percutaneous Balloon Mitral Valvuloplasty).[7] Si este procedimiento falla, puede ser necesario someterse a una cirugía de la válvula mitral, que puede implicar el reemplazo de la válvula, la reparación o una comisurotomía.[7] Se recomienda la anticoagulación para los pacientes que tienen estenosis mitral en el marco de una fibrilación auricular o de un evento embólico previo.[7] No se requiere ninguna terapia para los pacientes asintomáticos. Los diuréticos pueden ser usados para tratar la congestión pulmonar o el edema.[13]
Regurgitación mitral
[editar]Se recomienda la cirugía para la regurgitación mitral crónica grave en pacientes sintomáticos con una fracción de eyección del ventrículo izquierdo (FEVI) superior al 30 %, y en pacientes asintomáticos con un FEVI del 30-60 % o un volumen diastólico final del ventrículo izquierdo (VDFVI) > del 40 %.[7] Se prefiere la reparación quirúrgica de las valvas a la sustitución de la válvula mitral siempre que la reparación sea factible.[7]
La regurgitación mitral puede ser tratada médicamente con vasodilatadores, diuréticos, digoxina, antiarrítmicos y anticoagulación crónica.[12][13] La regurgitación mitral de leve a moderada debe ser seguida con ecocardiografía y prueba de esfuerzo cardíaco cada 1-3 años.[12] La regurgitación mitral severa debe ser seguida con ecocardiografía cada 3-6 meses.[12]
Epidemiología
[editar]En Estados Unidos, alrededor del 2,5 % de la población tiene una enfermedad cardíaca valvular de moderada a grave.[25] La prevalencia de estas enfermedades aumenta con la edad, y las personas de 75 años de edad en los Estados Unidos tienen una prevalencia de alrededor del 13 %.[25] En las regiones industrialmente subdesarrolladas, la enfermedad reumática es la causa más común de las enfermedades valvulares, y puede causar hasta el 65 % de los trastornos valvulares vistos en estas regiones.[25]
En España el número de afectados por alguna valvulopatía está en el 3 % de la población mayor de 65 años y en el 7,4 % en los mayores de 85 años.[26]
Estenosis aórtica
[editar]La estenosis aórtica es típicamente el resultado del envejecimiento, ocurriendo en el 12,4 % de la población mayor de 75 años de edad y representa la causa más común de obstrucción de salida en el ventrículo izquierdo.[1] Las válvulas aórticas bicúspides se encuentran en hasta el 1 % de la población, convirtiéndola en una de las anormalidades cardíacas más comunes.[27]
Regurgitación aórtica
[editar]La prevalencia de la regurgitación aórtica también aumenta con la edad. La enfermedad moderada a grave tiene una prevalencia del 13 % en pacientes de entre 55 y 86 años.[25] Esta enfermedad valvular es causada principalmente por la dilatación de la raíz aórtica, pero la endocarditis infecciosa ha sido un factor de riesgo creciente. Se ha encontrado que es la causa de la regurgitación aórtica en hasta el 25 % de los casos quirúrgicos.[25]
Estenosis mitral
[editar]La estenosis de la válvula mitral es causada casi exclusivamente por la enfermedad cardiaca reumática y tiene una prevalencia de alrededor del 0,1 % en los Estados Unidos.[25] La estenosis mitral es la enfermedad valvular del corazón más común en el embarazo.[28]
Regurgitación Mitral
[editar]La regurgitación mitral se asocia significativamente con el envejecimiento normal, aumentando su prevalencia con la edad. Se estima que está presente en más del 9 % de las personas mayores de 75 años.[1]
Referencias
[editar]- ↑ a b c d Burden of valvular heart diseases: a population-based study. Nkomo VT, Gardin JM, Skelton TN, Gottdiener JS, Scott CG, Enriquez-Sarano. Lancet. 2006 Sep;368(9540):1005-11.
- ↑ Pregnancy and contraception in congenital heart disease: what women are not told. Kovacs AH, Harrison JL, Colman JM, Sermer M, Siu SC, Silversides CK J Am Coll Cardiol. 2008;52(7):577.
- ↑ a b Bonow RO, Carabello BA, Kanu C, etal (2006). «ACC/AHA 2006 guidelines for the management of patients with valvular heart disease: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (writing committee to revise the 1998 Guidelines for the Management of Patients With Valvular Heart Disease): developed in collaboration with the Society of Cardiovascular Anesthesiologists: endorsed by the Society for Cardiovascular Angiography and Interventions and the Society of Thoracic Surgeons». Circulation 114 (5): e84-231. PMID 16880336. doi:10.1161/CIRCULATIONAHA.106.176857.
- ↑ a b Sociedad Española del Corazón: Ficha del paciente: Valvulopatía. Consultado el 25 de noviembre de 2016
- ↑ a b c Ragavendra R. Baliga, Kim A. Eagle, William F Armstrong, David S Bach, Eric R Bates, Practical Cardiology, Lippincott Williams & Wilkins, 2008, page 452.
- ↑ Chapter 1: Diseases of the Cardiovascular system > Section: Valvular Heart Disease in: Elizabeth D Agabegi; Agabegi, Steven S. (2008). Step-Up to Medicine (Step-Up Series). Hagerstwon, MD: Lippincott Williams & Wilkins. ISBN 0-7817-7153-6.
- ↑ a b c d e f g h i j k l m n 2014 AHA/ACC guideline for the management of patients with valvular heart disease: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. Nishimura RA, Otto CM, Bonow RO, Carabello BA, Erwin JP 3rd, Guyton RA, O'Gara PT, Ruiz CE, Skubas NJ, Sorajja P, Sundt TM 3rd, Thomas JD. J Am Coll Cardiol. 2014;63(22):e57.
- ↑ Isolated pulmonic valve infective endocarditis: a persistent challenge. Hamza N, Ortiz J, Bonomo. Infection. 2004 Jun;32(3):170-5.
- ↑ Carcinoid heart disease. Clinical and echocardiographic spectrum in 74 patients. Pellikka PA, Tajik AJ, Khandheria BK, Seward JB, Callahan JA, Pitot HC, Kvols LK. Circulation. 1993;87(4):1188.
- ↑ Recommendations for evaluation of the severity of native valvular regurgitation with two-dimensional and Doppler echocardiography. Zoghbi WA, Enriquez-Sarano M, Foster E, Grayburn PA, Kraft CD, Levine RA, Nihoyannopoulos P, Otto CM, Quinones MA, Rakowski H, Stewart WJ, Waggoner A, Weissman NJ, American Society of Echocardiography. J Am Soc Echocardiogr. 2003;16(7):777.
- ↑ Impact of tricuspid regurgitation on long-term survival. Nath J, Foster E, Heidenreich PA. J Am Coll Cardiol. 2004;43(3):405.
- ↑ a b c d e f g h i j k l m n ñ o p q r s t u VOC=VITIUM ORGANICUM CORDIS, a compendium of the Department of Cardiology at Uppsala Academic Hospital. By Per Kvidal September 1999, with revision by Erik Björklund May 2008
- ↑ a b c d e f g h i j k l m n ñ o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al am an añ ao ap aq ar as at au av aw ax ay Chapter 1: Diseases of the Cardiovascular system > Section: Valvular Heart Disease in: Elizabeth D Agabegi; Agabegi, Steven S. (2008). Step-Up to Medicine (Step-Up Series). Hagerstwon, MD: Lippincott Williams & Wilkins. ISBN 978-0-7817-7153-5.
- ↑ a b c Rosenhek R, Baumgartner H. Aortic Stenosis. In: Valvular Heart Disease, 4th, Otto CM, Bonow RO. (Eds), Saunders/Elsevier, Philadelphia 2013. pp 139-162.
- ↑ a b O'Gara, Patrick T.; Loscalzo, Joseph (13 de agosto de 2018). «Aortic Valve Disease». Harrison's principles of internal medicine. Jameson, J. Larry,, Kasper, Dennis L.,, Longo, Dan L. (Dan Louis), 1949-, Fauci, Anthony S., 1940-, Hauser, Stephen L.,, Loscalzo, Joseph (20th edición). New York. ISBN 978-1-259-64403-0. OCLC 1029074059.
- ↑ www.hca.es
- ↑ a b c d e O'Gara, Patrick T.; Loscalzo, Joseph. "Aortic Regurgitation". Harrison's principles of internal medicine. Jameson, J. Larry, Kasper, Dennis L., Longo, Dan L. (Dan Louis), 1949-, Fauci, Anthony S., 1940-, Hauser, Stephen L., Loscalzo, Joseph, (20th edition ed.). New York. ISBN 978-1-259-64403-0. OCLC 1029074059.
- ↑ a b c d O'Gara, Patrick T.; Loscalzo, Joseph. "Mitral Stenosis". Harrison's principles of internal medicine. Jameson, J. Larry,, Kasper, Dennis L.,, Longo, Dan L. (Dan Louis), 1949-, Fauci, Anthony S., 1940-, Hauser, Stephen L.,, Loscalzo, Joseph, (20th edition ed.). New York. ISBN 978-1-259-64403-0. OCLC 1029074059.
- ↑ a b c d O'Gara, Patrick T.; Loscalzo, Joseph. "Mitral Regurgitation". Harrison's principles of internal medicine. Jameson, J. Larry,, Kasper, Dennis L., Longo, Dan L. (Dan Louis), 1949-, Fauci, Anthony S., 1940-, Hauser, Stephen L., Loscalzo, Joseph, (20th edition ed.). New York. ISBN 978-1-259-64403-0. OCLC 1029074059.
- ↑ a b Owens DS, O'Brien KD. Clinical and Genetic Risk Factors for Calcific Valve Disease. In: Valvular Heart Disease, 4th, Otto CM, Bonow RO. (Eds), Saunders/Elsevier, Philadelphia 2013. pp.53-62.
- ↑ Schade R, Andersohn F, Suissa S, Haverkamp W, Garbe E (2007). «Agonistas de la dopamina y el riesgo de regurgitación de la válvula cardíaca». N. Engl. J. Med. 356 (1): 29-38. PMID 17202453. doi:10.1056/NEJMoa062222.
- ↑ a b Vinay, Kumar (2013). Robbin's Basic Pathology. Elsevier Health Sciences. pp. Chapter 10: Heart.
- ↑ a b c d e f g Bonow, RO; Carabello, BA; Chatterjee, K; De Leon Jr, AC; Faxon, DP; Freed, MD; Gaasch, WH; Lytle, BW et al. (2008). «2008 focused update incorporated into the ACC/AHA 2006 guidelines for the management of patients with valvular heart disease: A report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to revise the 1998 guidelines for the management of patients with valvular heart disease). Endorsed by the Society of Cardiovascular Anesthesiologists, Society for Cardiovascular Angiography and Interventions, and Society of Thoracic Surgeons». Journal of the American College of Cardiology 52 (13): e1-142. PMID 18848134. doi:10.1016/j.jacc.2008.05.007.
- ↑ Nishimura, Rick A.; Otto, Catherine M.; Bonow, Robert O.; Carabello, Blase A.; Erwin, John P.; Fleisher, Lee A.; Jneid, Hani; Mack, Michael J.; McLeod, Christopher J.; O’Gara, Patrick T.; Rigolin, Vera H. (11 de julio de 2017). «2017 AHA/ACC Focused Update of the 2014 AHA/ACC Guideline for the Management of Patients With Valvular Heart Disease: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines». Journal of the American College of Cardiology 70 (2): 252-289. ISSN 0735-1097. PMID 28315732. doi:10.1016/j.jacc.2017.03.011.
- ↑ a b c d e f Chambers, John B.; Bridgewater, Ben (2014). «Epidemiology of Valvular Heart Disease». En Otto, CM; Bonow, RO, eds. Enfermedad del corazón valvular (4th edición) (Saunders). pp. 1-13.
- ↑ D, S. A. «Las valvulopatías cardiacas afectan al 3% de las personas mayores de 65 años en España - Salud a Diario». www.saludadiario.es. Consultado el 24 de junio de 2020.
- ↑ Braverman AC. La válvula aórtica bicúspide y la enfermedad aórtica asociada. En: Valvular Heart Disease, 4th, Otto CM, Bonow RO. (Eds), Saunders/Elsevier, Filadelfia 2013. p.179.
- ↑ Gelson, E.; Gatzoulis, M.; Johnson, M. (2007). «Valvular heart disease». BMJ (Clinical Research Ed.) 335 (7628): 1042-1045. PMC 2078629. PMID 18007005. doi:10.1136/bmj.39365.655833.AE.
