Formiato de metilo
| Formiato de metilo | ||
|---|---|---|
 | ||
 | ||
 | ||
| General | ||
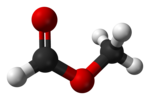
| Fórmula estructural |
 | |
| Fórmula molecular | C2H4O2 | |
| Identificadores | ||
| Número CAS | 107-31-3[1] | |
| Número RTECS | LQ8925000 | |
| ChEBI | 77699 | |
| ChEMBL | CHEMBL295026 | |
| ChemSpider | 7577 | |
| PubChem | 7865 | |
| UNII | 1MPH591FTG | |
| Propiedades físicas | ||
| Masa molar | 60,021 g/mol | |
El formiato de metilo, también llamado metanoato de metilo, es el éster metílico del ácido fórmico. Es el ejemplo más sencillo de éster de carboxilato y es un líquido incoloro con olor etéreo, alta presión de vapor y baja tensión superficial. Es un precursor de muchos otros compuestos de interés comercial.[2]
Producción
[editar]En el laboratorio, el formiato de metilo puede producirse mediante la reacción de condensación del metanol y el ácido fórmico, como sigue
HCOOH + CH3OH → HCOOCH3 + H2O
Sin embargo, el formiato de metilo industrial suele producirse mediante la combinación de metanol y monóxido de carbono (carbonilación) en presencia de una base fuerte, como el metóxido de sodio:[2]

Este proceso, practicado comercialmente por BASF entre otras empresas, ofrece una selectividad del 96% hacia el formiato de metilo. El catalizador de este proceso es sensible al agua, que puede estar presente en la materia prima de monóxido de carbono, que suele proceder del gas de síntesis. Por lo tanto, es esencial que el monóxido de carbono esté muy seco.[3]
Usos
[editar]El formiato de metilo se utiliza principalmente para fabricar formamida, dimetilformamida y ácido fórmico. Estos compuestos son precursores o componentes básicos de muchos derivados útiles.
Debido a su alta presión de vapor, se utiliza para acabados de secado rápido y como agente espumante para algunas aplicaciones de espuma de poliuretano y como sustituto de CFC, HCFC y HFC. El formiato de metilo tiene un potencial cero de agotamiento de la capa de ozono y un potencial cero de calentamiento global. También se utiliza como insecticida.
Un uso histórico del formiato de metilo, que a veces llama la atención, fue en la refrigeración. Antes de la introducción de refrigerantes menos tóxicos, el formiato de metilo se utilizaba como alternativa al dióxido de azufre en los frigoríficos domésticos.
Referencias
[editar]- ↑ Número CAS
- ↑ a b Werner Reutemann and Heinz Kieczka "Formic Acid" in Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. doi 10.1002/14356007.a12_013
- ↑ W. Couteau, J. Ramioulle, US Patent US4216339
Enlaces externos
[editar]- NIST Chemistry WebBook: Methyl formate
- ChemicalLand21.com entry on METHYL FORMATE
- CDC - NIOSH Pocket Guide to Chemical Hazards
- Esta obra contiene una traducción derivada de «Methyl formate» de Wikipedia en inglés, concretamente de esta versión, publicada por sus editores bajo la Licencia de documentación libre de GNU y la Licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional.
